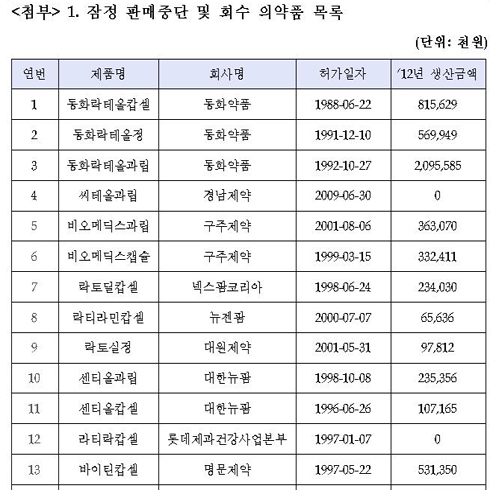
▲사진=잠정 판매 중단 및 회수 조치 의약품 제품 일부 목록 [제공/식품안전처]
[투데이코리아=송한솔 기자] 식품의약품안전처는 8일 “동화약품 락테올 등이 정부로부터 허가받은 급성설사에 대한 효능, 효과 등이 충분히 입증되지 않은 것으로 확인돼 잠정 판매중단 및 회수 조치를 취하기로 했다”고 밝혔다.
락테올 허가 당시 제출된 균주(틴달화락토바실루스아시도필루스)와 현재 실제 제품 생산에 쓰이는 균주(퍼멘텀 균주와 델브뤼키 균주 혼합물)가 다른 사실이 확인됐기 때문이다.
식약처 조사 결과, 동화약품은 락테올을 제조하면서 지난 1988년 허가 당시 제출된 ‘틴달화 아시도필루스’ 균주가 아닌 다른 유산균을 사용한 것으로 드러났다. 특히 동화약품은 지난 2005년 프랑스 원개발사로부터 유산균이 달라졌다는 내용을 통보받고도 식약처에 변경신고 절차를 진행하지 않았다.
앞으로 동화약품은 식약처 주관으로 락테올캡슐, 락테올정, 락테올과립 등 3개 품목에 대하여 특별재평가를 받게 된다. 평가방법은 프랑스 허가자료, 품질검사 등을 조사·평가하게 되며, 중앙약사심의위원회 자문을 거쳐 이르면 오는 10월말까지 후속조치가 나올 예정이다. 식약처는 이번 특별 재평가와 더불어 재발 방지를 위한 제도개선을 추진할 계획이다.
식약처는 일선 약국에서 락테올과 제네릭 제품의 반품이 원활히 진행될 수 있도록 약사회, 제약협회, 도매협회 및 해당 제약사에 협조 요청할 계획이다.
기존에 급성설사 증상 때문에 동 제네릭 제품을 복용하던 환자들은 의·약사와 상담해 시중에 공급되고 있는 일반 지사제나 다른 유산균제제를 복용하면 된다.
식약처는 향후 유산균 제제의 관리강화를 위해 유산균제제의 허가신청 시 유산균의 균종 입증자료 등을 제출토록 '의약품의 품목허가·신고·심사규정'을 개정할 계획이다.
또한 모든 유산균종에 대해 확인시험법(PCR, 종 특이적 시험법)을 추가, 정기적으로 유산균종을 확인할 수 있도록 품질관리를 강화할 방침이다.
- 기자명 송한솔 기자
- 승인시간 2013.08.08 13:49
- 수정시간 2013.08.08 13:49
- 댓글 0

